国家食品药品监督管理局发布的第一类医疗器械产品目录和相应体外诊断试剂分类子目录中的第一类医疗器械。
国产一类医疗器械备案办理条件
国家食品药品监督管理局发布的第一类医疗器械产品目录和相应体外诊断试剂分类子目录中的第一类医疗器械。
国产一类医疗器械备案申请材料清单
- 一类医疗器械备案表
- 安全风险分析报告
- 产品技术要求
- 产品检验报告
- 临床评价资料
- 产品说明书及最小销售单元标签设计样稿
- 生产制造信息
- 营业执照(A类有限责任公司)
- 符合性声明
- 授权委托书
国产一类医疗器械备案办理依据
-
- 法律法规名称:《医疗器械监督管理条例》
- 依据文号:2017年国务院令第680号修订第十条
-
- 法律法规名称:《医疗器械注册管理办法》2014年
- 依据文号:(国家食品药品监督管理总局令第4号)第六十条
-
- 法律法规名称:《医疗器械注册管理办法》、第五十九条
- 依据文号:2014年国家食品药品监督管理总局令第4号
-
- 法律法规名称:《医疗器械注册管理办法》
- 依据文号:国家食品药品监督管理局总局令第4号第五条、第五十七条、第五十八条、第五十九条、第六十条
华才检测相关服务
产品技术要求审核
产品临床评价资料审核
产品标签,说明书,包装文件审核
产品检测要求确定
产品备案资料编写与定稿
产品技术要求确认
产品备案资料递交
国产一类医疗器械备案咨询服务流程
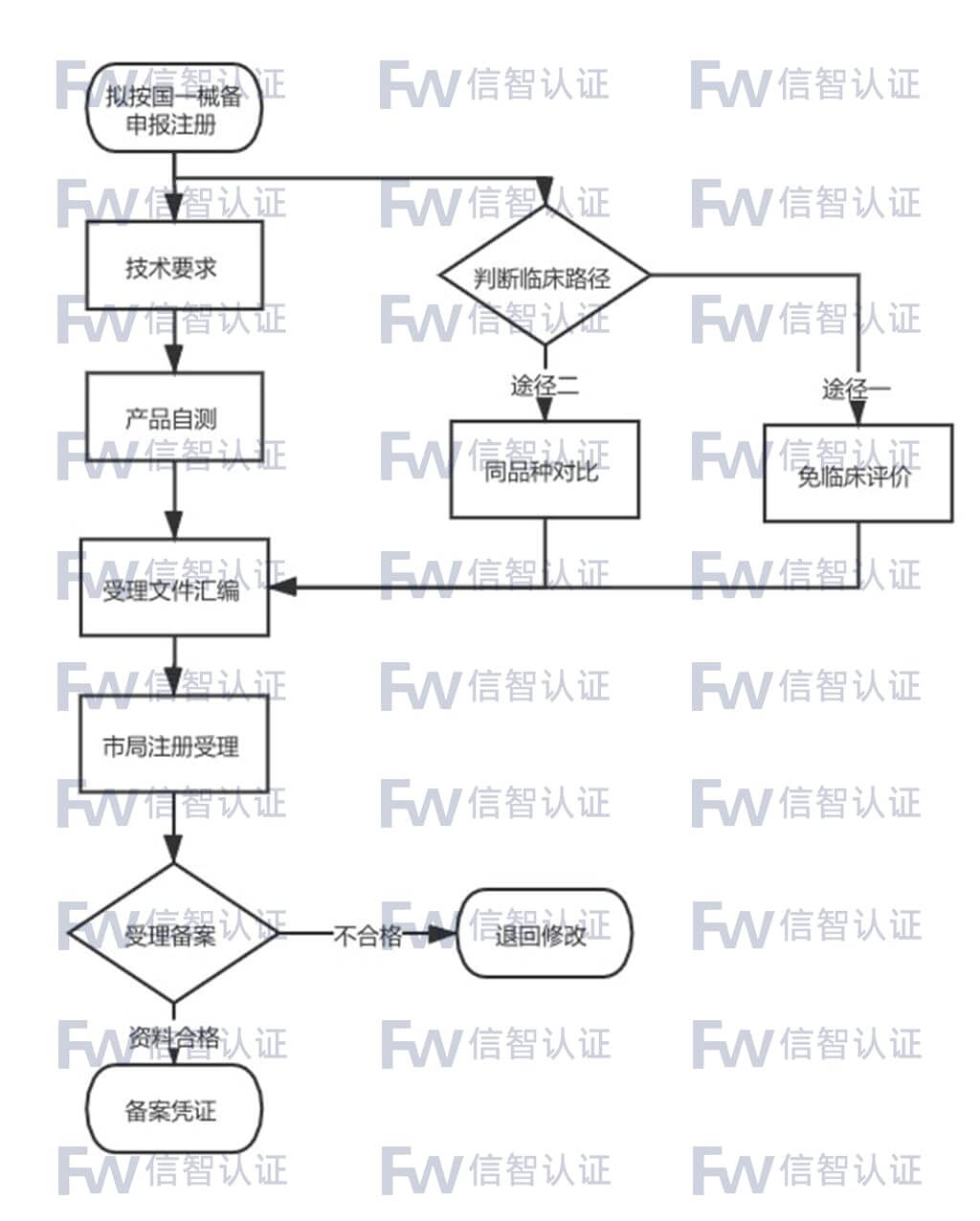
国产一类医疗器械备案官方收费
无

